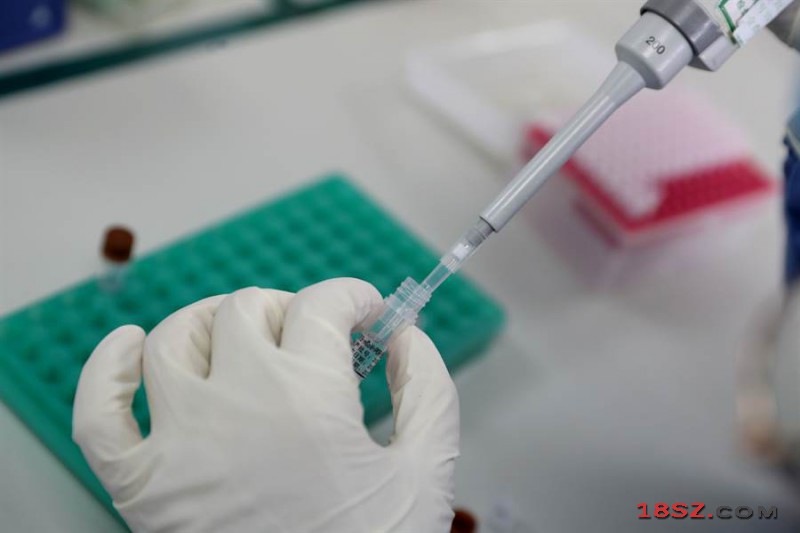
多家中企出口新冠病毒检测试剂品质差遭致批评,政府下令收紧药品生产出口管制。图为配制新冠病毒检测试剂。(图/新华社)
因多家中企出口检测试剂品质差遭致批评后,政府下令收紧药品生产出口管制,原先仅具海外销售资格便可出口的药品商,现已通知出口证取消,严格规定需要获得国家GMP出口认证才准予外销,许多药商表示将向商务部与药监局申诉。
据《廿一世纪经济报导》指出,昨日,中国药监局药品监管司召开了2020年药品监管工作会议,决定严格规范药品出口证明管理,对不符合出证条件和要求、未遵守药品GMP等情形,撤销其药品出口证明。商务部、海关总署、国家药监局联合发文,自4月1日起,出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的企业向海关报关时,须提供书面或电子声明,承诺出口产品已取得医疗器械产品注册证书,符合进口国(地区)的品质标准要求。
报导说,一位诊断试剂企业负责人透露,目前已经有多家企业收到通知被取消原有的出口许可证。一位业内资深人士指出,几个部委出台新规,导火线是「易瑞生物」公司,虽然大陆对抗疫物资品质一直要求严格,对出口产品也很重视,但是,「对于出口的检测试剂等物资,国外并未明确要求企业需要提供国内注册批文,而未获药监局的注册批文,只要有欧盟CE认证,也能允许出口欧洲国家。」
业者指出,出口许可证被通知取消了,原来出口只需要拿到海外销售资质就可以,现在直接受到影响了,我们打算向商务部申诉,希望不要一刀切。」
近期有媒体报导称,西班牙卫生部在中国大陆购买的易瑞生物快速检测试剂盒品质不合格。易瑞生物在其官网发布声明称,假阴性的出现不排除因验证时的操作流程、病人病歷、採样等事项导致结果偏差的可能,具体原因双方仍在沟通核实。
但据《21世纪经济报导》指出,确实有多家中国企业获得欧盟认证并进行销售,但却未获得中国的注册证,例如易瑞生物就未取得新型冠状病毒相关检测试剂产品注册批文。资深业内人士称,早在3月16日,药监局即已要求出口疫情物资必须要拿到药监局的证才能对外销售。而此一事件让药监局对新批试剂盒等抗疫物资更加谨慎,严格要求品质把关,以防类似易瑞生物事件出现。

 Iteca Exhibitions
Iteca Exhibitions 长城润滑油
长城润滑油 German Machine Tool Builders Association
German Machine Tool Builders Association 延长石油
延长石油 3M制造业
3M制造业 陕煤化工集团
陕煤化工集团 HUAWEI
HUAWEI Dahua Technology
Dahua Technology 中国石油
中国石油 Gemtique
Gemtique KUNVII
KUNVII PALEXPO
PALEXPO IAA Show
IAA Show LASTON
LASTON 中杭贸易
中杭贸易 Etek Europe
Etek Europe PV EXPO
PV EXPO QIIE青岛进博会
QIIE青岛进博会 陕西有色金属
陕西有色金属 维远光伏产业
维远光伏产业 Time Out Group
Time Out Group IFEMA
IFEMA 天元化工
天元化工 National Media
National Media 吉祥星科技
吉祥星科技 Dowpol Chemical
Dowpol Chemical 海康威视-HIK VISION
海康威视-HIK VISION Hannover Messe
Hannover Messe TOSHIBA
TOSHIBA Productronica
Productronica HealthCare
HealthCare 深圳会展中心
深圳会展中心 大唐旗舰店
大唐旗舰店 Soul Game
Soul Game 神木职教中心
神木职教中心 Sinopec
Sinopec 2019年美国康涅狄格国际视频游戏展览会
2019年美国康涅狄格国际视频游戏展览会 2023 NAB Show Centennial
2023 NAB Show Centennial EUROGUSS 2024
EUROGUSS 2024 宝能第一空间:致敬长征英雄 追寻东纵精神
宝能第一空间:致敬长征英雄 追寻东纵精神 勇敢的白衣战士 致敬最美逆行者
勇敢的白衣战士 致敬最美逆行者 异形珍珠《水母的舞蹈》视频欣赏
异形珍珠《水母的舞蹈》视频欣赏 世卫组织警告:部分国家对新冠肺炎疫情准备不足
世卫组织警告:部分国家对新冠肺炎疫情准备不足 白雪石三幅高价拍卖作品
白雪石三幅高价拍卖作品 China Forged Valves Factory Tour
China Forged Valves Factory Tour 2019年美国太空科技博览会
2019年美国太空科技博览会 第32届中国电影金鸡奖颁奖典礼举行
第32届中国电影金鸡奖颁奖典礼举行 AGFRC Products in FASZINATION MODELLBAU
AGFRC Products in FASZINATION MODELLBAU 河北静志寺地宫出土瓷器欣赏
河北静志寺地宫出土瓷器欣赏 厦门筼筜湖生态-蝶变
厦门筼筜湖生态-蝶变 2020印度嵌入式展设计图
2020印度嵌入式展设计图 2019年埃森国际野外旅游展览会
2019年埃森国际野外旅游展览会 Facial tissue
Facial tissue InterBee 2020(日本广电展会)线上展
InterBee 2020(日本广电展会)线上展 日本日立葫芦牌截止阀 进口HITACHI截止阀
日本日立葫芦牌截止阀 进口HITACHI截止阀 2025越南平阳国际铝工业展览会
2025越南平阳国际铝工业展览会 2024第四十四届深圳国际医疗器械展览会
2024第四十四届深圳国际医疗器械展览会 京剧人物油画
京剧人物油画 2024深圳国际数字能源展
2024深圳国际数字能源展 2023年第23届韩国釜山国际海事展
2023年第23届韩国釜山国际海事展 意大利里米尼城市介绍
意大利里米尼城市介绍 纽伦堡 - 玩具都城
纽伦堡 - 玩具都城 慕尼黑 - 伊萨尔河畔的酒都
慕尼黑 - 伊萨尔河畔的酒都 法兰克福 - 欧洲金融中心
法兰克福 - 欧洲金融中心 迪拜 - Dubal
迪拜 - Dubal 俄罗斯 - 战斗民族和套娃的国家
俄罗斯 - 战斗民族和套娃的国家 葡萄牙 - 软木塞之乡
葡萄牙 - 软木塞之乡 西班牙 - 斗牛士的故乡
西班牙 - 斗牛士的故乡





