
据央视新闻客户端消息,中国国家药监局今天发布通告,批准南京诺唯赞、北京金沃夫、深圳华大因源、广州万孚生物、北京华科泰生物的新冠抗原产品自测应用申请变更。自此五款新冠抗原自测产品正式上市。
根据中国国家药监局政务门户网站发布的最新待领取信息显示,四款新冠抗原检测试剂盒产品获得的医疗器械批准证明文件(变更)待领取,批准时间均在今天(12日),涉及四家公司,包括南京诺唯赞生物科技股份有限公司全资子公司南京诺唯赞医疗科技有限公司、广州万孚生物技术股份有限公司、华大基因子公司深圳华大因源医药科技有限公司、北京金沃夫生物工程科技有限公司。
加上前一天获准变更的北京华科泰,获准变更的厂商已经增至五家。

目前,中国共有五家企业的五款新冠抗原检测产品获批,正是上述五款变更信息的产品。此前,这些产品仅获批用于专业人员使用,而不能自测。
中国国家卫健委昨天宣布,国务院应对新冠疫情联防联控机制综合组决定在核酸检测基础上,增加抗原检测作为补充,并组织制定了《新新冠毒抗原检测应用方案(试行)》。
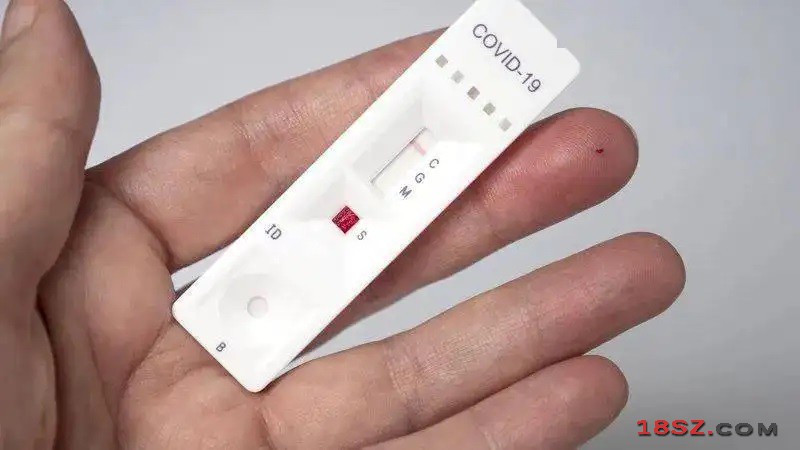
《方案》规定了抗原检测的适用人群:一是到基层医疗卫生机构就诊,伴有呼吸道、发热等症状且出现症状五天以内的人员;二是隔离观察人员,包括居家隔离观察、密接和次密接、入境隔离观察、封控区和管控区内的人员;三是有抗原自我检测需求的社区居民。
同时,《方案》明确了三类人群进行抗原检测需满足的主要条件、检测试剂的获得渠道,制定了检测发现阳性后的处置管理流程,促进抗原检测与核酸检测相衔接。为便于各地规范开展检测,《方案》还包括两个附件,即基层医疗卫生机构新冠病毒抗原检测基本要求及流程、新冠病毒抗原自测基本要求及流程。

受此消息影响,新冠检测概念股昨天直线拉升,新冠检测指数大涨8.16%。截至昨天收盘,体外诊断指数涨近8%,医药商业指数、肺炎主题指数、医疗器械指数涨幅均居前列。

 Iteca Exhibitions
Iteca Exhibitions 长城润滑油
长城润滑油 German Machine Tool Builders Association
German Machine Tool Builders Association 延长石油
延长石油 3M制造业
3M制造业 陕煤化工集团
陕煤化工集团 HUAWEI
HUAWEI Dahua Technology
Dahua Technology 中国石油
中国石油 Gemtique
Gemtique KUNVII
KUNVII PALEXPO
PALEXPO IAA Show
IAA Show LASTON
LASTON 中杭贸易
中杭贸易 Etek Europe
Etek Europe PV EXPO
PV EXPO QIIE青岛进博会
QIIE青岛进博会 陕西有色金属
陕西有色金属 维远光伏产业
维远光伏产业 Time Out Group
Time Out Group IFEMA
IFEMA 天元化工
天元化工 National Media
National Media 吉祥星科技
吉祥星科技 Dowpol Chemical
Dowpol Chemical 海康威视-HIK VISION
海康威视-HIK VISION Hannover Messe
Hannover Messe TOSHIBA
TOSHIBA Productronica
Productronica HealthCare
HealthCare 深圳会展中心
深圳会展中心 大唐旗舰店
大唐旗舰店 Soul Game
Soul Game 神木职教中心
神木职教中心 Sinopec
Sinopec 量子力学在近代技术中得到广泛应用
量子力学在近代技术中得到广泛应用 International trade fair for joining technology
International trade fair for joining technology 2023 NAB Show Centennial
2023 NAB Show Centennial 2019年瑞典国际军工及技术展览会
2019年瑞典国际军工及技术展览会 2021圣诞前夕宝能第一空间崔培鲁画展
2021圣诞前夕宝能第一空间崔培鲁画展 鸿华物流运输车
鸿华物流运输车 2019十大考古新发现推介:山东滕州西孟庄遗址
2019十大考古新发现推介:山东滕州西孟庄遗址 深美闳约-名家书画联展相聚宝能第一空间
深美闳约-名家书画联展相聚宝能第一空间 俄罗斯发现巨大绿宝石 总重量达4.8公斤
俄罗斯发现巨大绿宝石 总重量达4.8公斤 FACTORY PICTURES
FACTORY PICTURES 唐三彩美女
唐三彩美女 德国科隆狂欢节举办“玫瑰星期一”大游行
德国科隆狂欢节举办“玫瑰星期一”大游行 第七届丝博会现代农业馆宝鸡展区设计
第七届丝博会现代农业馆宝鸡展区设计 Exhibit at Achem Asia
Exhibit at Achem Asia 2019年欧洲国际聚氨酯及技术展览会
2019年欧洲国际聚氨酯及技术展览会 长春税务学院图书馆
长春税务学院图书馆 2024上海医疗器械展览会
2024上海医疗器械展览会 2024广州美博会&2024广州春季美博会展位预订咨询
2024广州美博会&2024广州春季美博会展位预订咨询 滚塑水塔
滚塑水塔 2023深圳国际酒店用品展览会
2023深圳国际酒店用品展览会 北京孕婴童用品展|2025年第36届京正北京孕婴童产业博览会
北京孕婴童用品展|2025年第36届京正北京孕婴童产业博览会 北京物联网展普通标展国外预订
北京物联网展普通标展国外预订 国画葡萄-醇香可掬
国画葡萄-醇香可掬 洛阳瑞克RGP300S受用户青睐订购
洛阳瑞克RGP300S受用户青睐订购 意大利里米尼城市介绍
意大利里米尼城市介绍 纽伦堡 - 玩具都城
纽伦堡 - 玩具都城 慕尼黑 - 伊萨尔河畔的酒都
慕尼黑 - 伊萨尔河畔的酒都 法兰克福 - 欧洲金融中心
法兰克福 - 欧洲金融中心 迪拜 - Dubal
迪拜 - Dubal 俄罗斯 - 战斗民族和套娃的国家
俄罗斯 - 战斗民族和套娃的国家 葡萄牙 - 软木塞之乡
葡萄牙 - 软木塞之乡 西班牙 - 斗牛士的故乡
西班牙 - 斗牛士的故乡





